- 2015-06-15 15:26
- 作者:佚名
- 来源:中国数字医疗网
七、我国医疗电子产业政策环境
(一)政策概述
2014 年是我国医疗电子产业发展的政策年,产业发展得到国家领导层高度重视,国务院、国家卫计委、国家食品药品监督管理总局等先后出台了多项有关推动医疗电子产业蓬勃发展的政策法规。
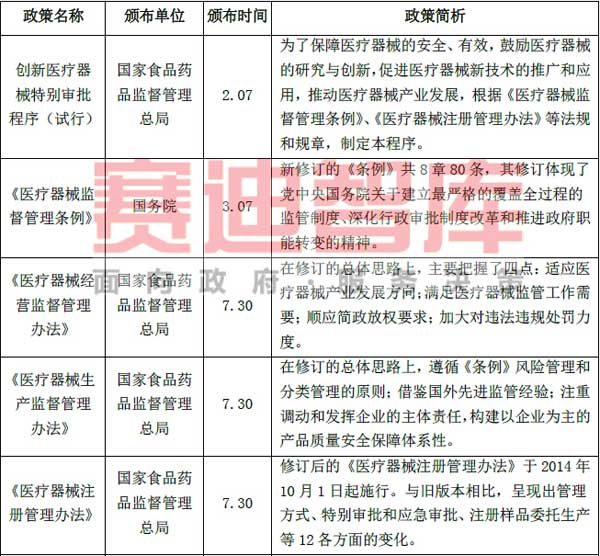
表22 医疗电子相关国家政策
(二)政策解析
1.《医疗器械监督管理条例》
新修订《条例》在完善分类管理、适当减少事前许可、加大生产经营企业和使用单位的责任、强化日常监管、完善法律责任等方面做出了较大修改。
一是明确对医疗器械按照风险程度实行分类管理,按风险从低到高将医疗器械分为一、二、三类。第一类医疗器械实行产品备案管理,第二类、第三类医疗器械实施产品注册管理。
二是加大了医疗器械生产经营企业在产品质量方面的控制责任,建立了经营和使用环节的进货查验及销售记录制度,增设了使用单位的医疗器械安全管理责任。同时,强化了监管部门的日常监管职责,规范了延续注册、抽检等监管行为,并通过增设医疗器械不良事件监测制度、已注册医疗器械再评价制度、医疗器械召回制度等,健全了管理制度,充实了监管手段。
三是明确提出国家鼓励医疗器械的研究与创新,促进医疗器械新技术的推广和应用,推动医疗器械产业的发展。
2.《医疗器械经营监督管理办法》
《医疗器械经营监督管理办法》作为新《条例》的配套规章之一,在修订的总体思路上,主要把握了以下四点:一是适应医疗器械产业发展方向;二是满足医疗器械监管工作需要;三是顺应简政放权要求;四是加大对违法违规处罚力度。
该办法修订体现了坚持分类管理、坚持企业主体责任、坚持严格监管、坚持追踪溯源等4 项原则。
该办法对企业经营质量管理方面提出了两项核心要求:一是强化了企业质量责任;二是更加注重经营全过程的质量管理。
同时,对为其他医疗器械生产经营企业提供贮存、配送服务的经营企业应当具备的条件、第一类医疗器械经营企业应当具备什么条件、医疗器械批发与零售企业的区别、对经营第三类医疗器械的特殊要求、医疗器械经营企业分立与合并后需要办理手续、医疗器械注册人及备案人或者生产企业销售医疗器械相关规定等各个方面也作出了详细的规定。
3.《医疗器械生产监督管理办法》
该办法作为《医疗器械监督管理条例》的配套规章之一,在修订的总体思路上,一是遵循《条例》风险管理和分类管理的原则;二是借鉴国外先进监管经验;三是结合我国现阶段经济社会的市场成熟度和社会诚信体系情况。
新修订的生产办法体现了风险管理、落实责任、强化监管、违法严处4 项原则。
办法对开办医疗器械生产企业提出了前置条件:一是有与生产的医疗器械相适应的生产场地、环境条件、生产设备以及专业技术人员;二是有对生产的医疗器械进行质量检验的机构或者专职检验人员以及检验设备;三是有保证医疗器械质量的管理制度;四是有与生产的医疗器械相适应的售后服务能力;五是符合产品研制、生产工艺文件规定的要求。
4.《医疗器械注册管理办法》
修订后的《医疗器械注册管理办法》于2014 年10 月1 日起施行,该办法与旧版本相比,在管理方式、特别审批和应急审批、注册样品委托生产、新研制的尚未列入分类目录的医疗器械、审批时限、注册检验、临床试验要求、技术审评环节、明确注册事项变更、注册证有效期、延续注册、管理类别等12 个方面进行了调整。
5.《关于推进医疗机构远程医疗服务的意见》
随着技术的进步,远程医疗服务的范围已经有了很大扩展,远程病理诊断、远程影像诊断、远程监护等新的远程医疗服务项目得到比较广泛的应用,原有的管理要求已经不能适应当前远程医疗服务发展的实际要求。为推动远程医疗服务持续健康发展,优化医疗资源配置,实现优质医疗资源下沉,国家卫生计生委制定了《关于推进医疗机构远程医疗服务的意见》。
《意见》明确,非医疗机构不得开展远程医疗服务;第三方机构可以为远程医疗服务提供平台,但不能直接开展服务;医疗机构间开展远程医疗服务,邀请方应当向患方充分告知,并征得其书面同意。《意见》还对远程医疗的管理规范、实施程序、责任认定、监督管理等作出明确规定。
| 共8页: 上一页 [1][2][3][4][5][6]7 [8]下一页 [查看全文] |